Sinónimos
- Carbohidratos o hidratos de carbono: Ha habido intentos para sustituir el término de hidratos de carbono. Desde 1996 el Comité Conjunto de la Unión Internacional de Química Pura y Aplicada (International Union of Pure and Applied Chemistry1 ) y de la Unión Internacional de Bioquímica y Biología Molecular (International Union of Biochemistry and Molecular Biology) recomienda el término carbohidrato y desaconseja el de hidratos de carbono.
- Glúcidos: Este nombre proviene de que pueden considerarse derivados de la glucosa por polimerización y pérdida de agua. El vocablo procede del griego "glycýs", que significa dulce.
- Azúcares: Este término sólo puede usarse para los monosacáridos (aldosas y cetosas) y los oligosacáridos inferiores (disacáridos). En singular (azúcar) se utiliza para referirse a lasacarosa o azúcar de mesa.
- Sacáridos: Proveniente del griego σάκχαρον que significa "azúcar". Es la raíz principal de los tipos principales de glúcidos (monosacáridos, disacáridos, oligosacáridos y polisacáridos).

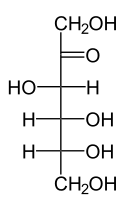
Glucosa-forma dextrogira Fructuosa-forma dextrogira
El término "hidrato de carbono" o "carbohidrato" es poco apropiado, ya que estas moléculas no son átomos de carbono hidratados, es decir, enlazados a moléculas de agua, sino que constan de átomos de carbono unidos a otros grupos funcionales como carbonilo ehidroxilo. Este nombre proviene de la nomenclatura química del siglo XIX, ya que las primeras sustancias aisladas respondían a la fórmula elemental Cn(H2O)n (donde "n" es un entero >= 3).
Los carbohidratos básicos o azúcares simples se denominan monosacáridos. Azúcares simples pueden combinarse para formar carbohidratos más complejos. Los carbohidratos con dos azúcares simples se llaman disacáridos. Carbohidratos que consisten de dos a diez azúcares simples se llaman oligosacáridos, y los que tienen un número mayor se llaman polisacáridos.
Los monosacáridos son azúcares simples
Clasificación de monosacáridos basado en el número de carbonos
| Número de Carbonos | Categoría | Ejemplos |
|---|---|---|
| 4 | Tetrosa | Eritrosa, Treosa |
| 5 | Pentosa | Arabinosa, Ribosa, Ribulosa, Xilosa, Xilulosa, Lixosa |
| 6 | Hexosa | Alosa, Altrosa, Fructosa, Galactosa, Glucosa, Gulosa, Idosa, Manosa, Sorbosa, Talosa, Tagatosa |
| 7 | Heptosa | Sedoheptulosa, Manoheptulosa |
Las estructuras de los sacáridos se distinguen principalmente por la orientación de los grupos hidroxilos (-OH). Esta pequeña diferencia estructural tiene un gran efecto en las propiedades bioquímicas, las características organolepticas (e.g., sabor), y en las propiedades físicas como el punto de fusión y la rotación específica de la luz polarizada. Un monosacárido de forma lineal que tiene un grupo carbonilo (C=O) en el carbono final formando un aldehído (-CHO) se clasifica como una aldosa. Cuando el grupo carbonilo está en un átomo interior formando una cetona, el monosacárido se clasifica como una cetosa.
Tetrosas
 |  |
| D-Eritrosa | D-Treosa |
Pentosas
 |  |  | 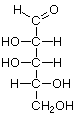 |
| D-Ribosa | D-Arabinosa | D-Xilosa | D-Lixosa |
La forma anular de la ribosa es un componente del ácido ribonucleico (ARN). La desoxirribosa, que se distingue de la ribosa por no tener un oxígeno en la posición 2, es un componente del ácido desoxirribonucleico (ADN). En los ácidos nucleicos, el grupo hidroxilo en el carbono numero 1 se reemplaza con bases nucleótidas.
 |  |
| Ribosa | Desoxirribosa |
Hexosas
Hexosas, como las que están ilustradas aquí, tienen la fórmula molecular C6H12O6. El químico alemán Emil Fischer (1852-1919) identificó los estereoisómeros de estas aldohexosas en 1894. Por este trabajo recibió un Premio Nobel en 1902.
 |  | 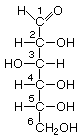 |  |
| D-Alosa | D-Altrosa | D-Glucosa | D-Manosa |
 |  | 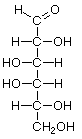 |  |
| D-Gulosa | D-Idosa | D-Galactosa | D-Talosa |
La glucosa, también llamadadextrosa, es el azúcar más predominante en las plantas y los animales, y es el azúcar presente en la sangre. La forma lineal de la glucosa es un aldehído polihídrico. En otras palabras, es una cadena de carbonos con varios grupos hidroxilos y un grupo aldehído. La fructosa, también llamada levulosa, está ilustrada aquí en forma lineal y anular. La relación entre estas formas se discute más tarde. La fructosa y la glucosa son los principales hidratos de carbono en la miel.
 | 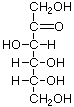 |  |  |  |
| D-Tagatosa (una cetosa) | D-Fructosa | Fructosa | Galactosa | Manosa |
Formas lineales y anulares
Los monosacáridos pueden existir en formas lineales y formas anulares, como se ha ilustrado anteriormente. La forma anular es más favorecida en soluciones acuosas, y el mecanismo de la formación de las formas cíclicas es semejante en todos los azúcares simples. La forma anular de la glucosa se crea cuando el oxígeno del carbono numero 5 se enlaza con el carbono que forma el grupo carbonilo (el carbono numero 1) y transfiere su hidrógeno al oxígeno del carbonilo para crear un grupo hidroxilo. Estos intercambios producen alfa-glucosa cuando el grupo hidroxilo resulta en el lado opuesto al grupo -CH2OH, o beta-glucosa cuando el grupo hidroxilo resulta en el mismo lado que el grupo -CH2OH. Isómeros como estos, que se diferencian solamente en la configuración del carbono del grupo carbonilo, se llaman anómeros. La letra Den el nombre se derivó originalmente de la propiedad de las soluciones de glucosa natural que desvían el plano de la luz polarizada a la derecha (dextrorotatoria), aunque ahora la letra denota una configuración específica. Monosacáridos que tienen formas cíclicas pentagonales, como la ribosa, se llaman furanosas. Azúcares con formas cíclicas hexagonales, como la glucosa, se llaman piranosas.
 | 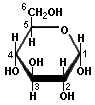 |  |  |
| D-Glucosa (una aldosa) | α-D-Glucosa | β-D-Glucosa | Ciclación de la glucosa |

CICLACIÓN DE LA GLUCOSA.
Los disacáridos son carbohidratos formados por dos azúcares simples.
Descripción y componentes de los disacáridos
| Disacárido | Descripción | Componentes |
|---|---|---|
| sucrosa | azúcar común | glucosa 1α→2 fructosa |
| maltosa | producto de la hidrólisis del almidón | glucosa 1α→4 glucosa |
| trehalosa | se encuentra en los hongos | glucosa 1α→1 glucosa |
| lactosa | el azúcar principal de la leche | galactosa 1β→4 glucosa |
| melibiosa | se encuentra en plantas leguminosas | galactosa 1α→6 glucosa |
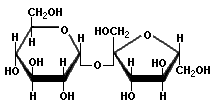 |  |  |
| Sucrosa | Lactosa | Maltosa |
La sucrosa (o sacarosa), es el azúcar común refinado de la caña de azúcar y la remolacha azucarera. La sucrosa es el carbohidrato principal del azúcar moreno, del azúcar tamizado, y de la melaza. La lactosa está formada por una molécula de glucosa y otra de galactosa. La intolerancia de lactosa es causada por una deficiencia de enzimas (lactasas) que desdoblan la molécula de lactosa en dos monosacáridos. La inhabilidad de digerir la lactosa resulta en la fermentación de este glúcido por bacterias intestinales que producen ácido láctico y gases que causan flatulencia, meteorismo, cólico abdominal, y diarrea. El yogur no causa estos problemas porque los microorganismos que transforman la leche en yogur consumen la lactosa.
La Maltosa consiste de dos moléculas de α-D-glucosa con el enlace alfa del carbono 1 de una molécula conectado al oxígeno en el carbono 4 de la segunda molécula. Esta unión se llama un enlace glicosídico 1α→4 (también se llama "enlace glucosídico" en muchos textos en español). La trehalosa consiste de dos moléculas de α-D-glucosa conectadas con un enlace 1α→1. La celobiosa es un disacárido formado por dos moléculas de β-D-glucosa conectadas por un enlace 1β→4 como la celulosa. La celobiosa no tiene sabor, mientras que la maltosa y la trehalosa son aproximadamente una tercera parte tan dulces como la sucrosa.
Trisacáridos
La rafinosa (o melitosa) es un trisacárido que se encuentra en muchas plantas leguminosas y crucíferas como los frijoles (judías), guisantes, col, y brócoli. La rafinosa está formada por una molécula de galactosa conectada a una de sucrosa por un enlace glicosídico 1α→6. Este sacárido es indigestible por los seres humanos y se fermenta en el intestino grueso por bacterias que producen gas. Tabletas que contienen la enzima alfa-galactosidasa, como el suplemento farmacéutico Beano, se usan frecuentemente para ayudar a la digestión y para evitar el meteorismo y flatulencias. La enzima se deriva de variedades comestibles del hongo Aspergillus niger.

Rafinosa
Los polisacáridos son polímeros de azúcares simples
Muchos polisacáridos, a diferencia de los azúcares, son insolubles en agua. La fibra dietética consiste de polisacáridos y oligosacáridos que resisten la digestión y la absorción en el intestino delgado, pero son completamente o parcialmente fermentados por microorganismos en el intestino grueso. Los polisacáridos que se describen a continuación son muy importantes en la nutrición, la biología, o la preparación de alimentos.
Almidón
El almidón es la forma principal de reservas de carbohidratos en los vegetales. El almidón es una mezcla de dos sustancias: amilosa, un polisacárido esencialmente lineal, yamilopectina, un polisacárido con una estructura muy ramificada. Las dos formas de almidón son polímeros de α-D-Glucosa. Los almidones naturales contienen 10-20% de amilosa y 80-90% de amilopectina. La amilosa forma una dispersión coloidal en agua caliente que ayuda a espesar caldos o salsas, mientras que la amilopectina es completamente insoluble.
- Las moléculas de amilosa consisten típicamente de 200 a 20,000 unidades de glucosa que se despliegan en forma de hélix como consecuencia de los ángulos en los enlaces entre las moléculas de glucosa.
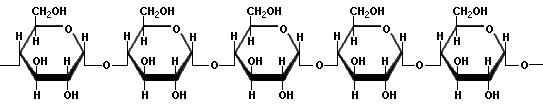
Amilosa - La amilopectina se distingue de la amilosa por ser muy ramificada. Cadenas laterales cortas conteniendo aproximadamente 30 unidades de glucosa se unen con enlaces 1α→6 cada veinte o treinta unidades de glucosa a lo largo de las cadenas principales. Las moléculas de amilopectina pueden contener hasta dos millones de unidades de glucosa.
 |
Amilopectina |
 |
| Las cadenas laterales se agrupan dentro de la molécula de amilopectina |
Los almidones se transforman en muchos productos comerciales por medio de hidrólisis usando ácidos o enzimas como catalizadores. La hidrólisis es una reacción química que desdobla cadenas largas de polisacáridos por la acción del agua para producir cadenas más pequeñas o carbohidratos simples. Los productos resultantes son asignados un valor de equivalencia en dextrosa (DE) que está relacionado al nivel de hidrólisis realizado. Un DE con valor de 100 corresponde al almidón completamente hidrolizado, que es la glucosa (dextrosa) pura. Las dextrinas son un grupo de carbohidratos producidos por la hidrolisis del almidón. Las dextrinas son polímeros de cadena corta que consisten de moléculas de D-glucosa unidas por enlaces glicosídicos 1α→4 o 1α→6. La maltodextrina es un almidón parcialmente hidrolizado que no es dulce y que tiene un valor DE menor de 20. Los jarabes, como el jarabe de maíz o miel de maíz, provienen del almidón de maíz y tienen valores DE de 20 a 91. La dextrosa comercial tiene valores DE de 92 a 99. Sólidos de jarabe de maíz son productos semicristalinos o polvos amorfos de poca dulzura con DE de 20 a 36 que se producen secando el jarabe de maíz al vacio o por atomización en cámara secadora. El jarabe de maíz de alta fructosa (JMAF), que se usa comúnmente en la producción de refrescos, se produce tratando el jarabe de maíz con enzimas que convierten una porción de la glucosa a fructosa. El jarabe de maíz de alta fructosa contiene aproximadamente 42% a 55% de fructosa y el resto consiste principalmente de glucosa. El almidón modificado es un almidón alterado por procesos mecánicos o químicos para estabilizar geles de almidón hechas con agua caliente. Sin modificación, geles de almidón y agua pierden su viscosidad o adquieren una textura plástica después de varias horas. Los jarabes de glucosa hidrogenados se producen hidrolizando almidón, y después hidrogenando el jarabe resultante para producir azúcar-alcoholes como el maltitol, el sorbitol, y otros oligo- y polisacáridos hidrogenados. La polidextrosa (poli-D-glucosa) es un polímero muy ramificado con muchos tipos de enlaces glicosídicos. Se produce calentando dextrosa con un catalizador ácido y purificando el resultante polímero soluble en agua. La polidextrosa se usa como voluminizador en productos alimenticios porque no tiene sabor y es semejante a la fibra en su resistencia a la digestión. El almidón resistente es almidón comestible que no se degrada en el estómago, pero se fermenta por la microflora en el intestino grueso.
Glucógeno (Glicógeno)
La glucosa se almacena como glucógeno en los tejidos del cuerpo por el proceso de glucogénesis. Cuando la glucosa no se puede almacenar como glucógeno o convertirse inmediatamente a energía, es convertida a grasa. El glucógeno es un polímero de α-D-Glucosa idéntico a la amilopectina, pero las ramificaciones son mas cortas (aproximadamente 13 unidades de glucosa) y más frecuentes. Las cadenas de glucosa están organizadas globularmente como las ramas de un árbol originando de un par de moléculas de glucogenina, una proteína con un peso molecular de 38,000 que sirve como cebador en el centro de la estructura. El glucógeno se convierte fácilmente en glucosa para proveer energía.
 |
| Glucógeno |
Dextranos
Los dextranos son polisacáridos semejantes a la amilopectina, pero las cadenas principales están formadas por enlaces glicosídicos 1α→6 y las cadenas laterales tienen enlaces 1α→3 o 1α→4. Las bacterias bucales producen dextranos que se adhieren a los dientes formando placa dental. Los dextranos tienen usos comerciales en la producción de dulces, lacas, aditivos comestibles, y voluminizadores del plasma sanguíneo.
 |
| Dextranos |
Inulina
Algunas plantas almacenan los hidratos de carbono no solamente como almidón sino también como inulina. Las inulinas se encuentran en muchos vegetales y frutas incluso las cebollas, ajo común, plátanos, papa de Jerusalén, y jícama. Las inulinas, tambien llamadas fructanos, son polímeros formados por cadenas de fructosa con una glucosa terminal. La oligofructosa tiene la misma estructura que la inulina, pero las cadenas tienen diez o menos unidades de fructosa. La oligofructosa tiene aproximadamente el 30 o el 50 por ciento de la dulzura del azúcar común. La inulina es menos soluble que la oligofructosa y tiene una textura cremosa que se siente como grasa en la boca. La inulina y la oligofructosa son indigestibles por las enzimas en los intestinos humanos, pero son totalmente fermentadas por los microorganismos intestinales. Los ácidos grasos de cadena corta y el lactato producido por la fermentación contribuyen 1.5 kcal por gramo de inulina u oligofructosa. La inulina y la oligofructosa se usan para reemplazar la grasa y el azúcar en alimentos como los helados, productos lácteos, dulces, y repostería.
 |
| Inulina n = aprox. 35 |
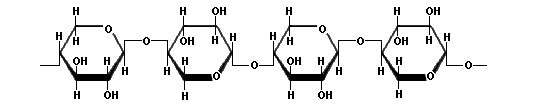
Celulosa
La celulosa es un polímero con cadenas largas sin ramificaciones de β-D-Glucosa y se distingue del almidón por tener grupos -CH2OH alternando por arriba y por debajo del plano de la molécula. La ausencia de cadenas laterales permite a las moléculas de celulosa acercarse unas a otras para formar estructuras rígidas. La celulosa es el material estructural más común en las plantas. La madera consiste principalmente de celulosa, y el algodón es casi celulosa pura. La celulosa puede ser desdoblada (hidrolizada) en sus glucosas constituyentes por microorganismos que residen en el sistema digestivo de las termitas y los rumiantes. La celulosa se puede modificar en el laboratorio tratándola con ácido nítrico (HNO3) para reemplazar todos los grupos hidroxilos con nitratos (-ONO2) y producir el nitrato de celulosa (nitrocelulosa o algodón explosivo) que es un componente de la pólvora sin humo. La celulosa parcialmente nitrada, piroxilina, se usa en la producción del colodión, plásticos, lacas, y esmaltes de uñas.
 | ||||||||||
CelulosaHemicelulosa
Las hemicelulosas son polisacáridos que, excluyendo la celulosa, constituyen las paredes celulares de las plantas y se pueden extraer con soluciones alcalinas diluidas. Las hemicelulosas forman aproximadamente una tercera parte de los carbohidratos en las partes maderosas de las plantas. La estructura química de las hemicelulosas consiste de cadenas largas con una gran variedad de pentosas, hexosas, y sus correspondientes ácidos úronicos. Las hemicelulosas se encuentran en frutas, tallos de plantas, y las cáscaras de granos. Aunque las hemicelulosas no son digeribles, pueden ser fermentadas por levaduras y bacterias. Los polisacáridos que producen pentosas al desdoblarse se llaman pentosanos. La xilana es un pentosano que consiste de unidades de D-xilosa conectadas por enlaces 1β→4.
Arabinoxilano
Los arabinoxilanos son polisacáridos que se encuentran en el salvado (la cubierta exterior de granos) como el trigo, el centeno, y la cebada. Los arabinoxilanos tienen un esqueleto químico de xilana con unidades de L-arabinofuranosa (L-arabinosa en su estructura pentagonal) distribuidas al azar con enlaces 1α→2 y 1α→3 a lo largo de la cadena de xilosas. Las xilosa y la arabinosa son ambas pentosas, por eso los arabinoxilanos también se clasifican como pentosanos. Los arabinoxilanos son de importancia en la panadería. Las unidades de arabinosa producen compuestos viscosos con el agua que afectan la consistencia de la masa, la retención de burbujas de la fermentación en las películas de gluten y almidón, y la textura final de los productos horneados.
 Clasificacion de las proteinas segun origen y estructura
La clasificacion de las proteinas puede hacerse teniendo en cuenta criterios diferentes: Por su Origen, por ejemplo, proteínas de origen animal: *Escleroproteínas o proteínas fibrosas: Como la elastina del músculo y el colágeno del tejido conjuntivo. Estas proteínas se caracterizan por su cualidad de insolubles gracias a su estructura molecular, y se encargan de cumplir funciones de protección y soporte de la mayor parte de los tejidos. Si bien no son digeribles, debemos decir que se aprovecha un producto derivado, el cual conocemos como la gelatina.
La clasificacion de las proteinas tambien puede hacerse por su Estructura:
1)- Simples y Haloproteinas: son las compuestas solo por aminoácido, forman cadena peptidicas. Por ejemplo: la albúmina.
2)- Complejas o Heteroproteinas: son las que se encuentran unidas a un grupo no proteico llamado grupo protetico, por ejemplo: lipoproteínas y nucleoproteínas.
 PROTEINAS SIMPLES:
Las proteínas simples constan sólo de aminoácidos o de sus derivados. Cuando se hidrolizan por ácidos, álcalis o enzimas, las proteínas simples producen aminoácidos únicos o sus derivados. Podemos nombrar los siguientes grupos.
Las proteínas conjugadas se incluyen el siguiente grupo.
Por sus propiedades físico-químicas, las proteínas se pueden
clasificar en proteínas simples (holoproteidos), que por hidrólisis dan solo
aminoácidos o sus derivados; proteínas conjugadas (heteroproteidos), que por
hidrólisis dan aminoácidos acompañados de sustancias diversas, y proteínas
derivadas, sustancias formadas por desnaturalización y desdoblamiento de las
anteriores. Las proteínas son indispensables para la vida, sobre todo por su
función plástica (constituyen el 80% del protoplasma deshidratado de toda
célula), pero también por sus funciones biorreguladoras (forma parte de las
enzimas) y de defensa (los anticuerpos son proteínas). Es la manera como se
organiza una proteína para adquirir cierta forma, presentan una disposición
característica en condiciones fisiológicas, pero si se cambian estas
condiciones como temperatura, pH, etc. pierde la conformación y su función,
proceso denominado desnaturalización. La función depende de la conformación y
ésta viene determinada por la secuencia de aminoácidos.
Para el estudio de la estructura es frecuente considerar una
división en cuatro niveles de organización, aunque el cuarto no siempre está
presente.
Conformaciones o niveles estructurales de la disposición
tridimensional:
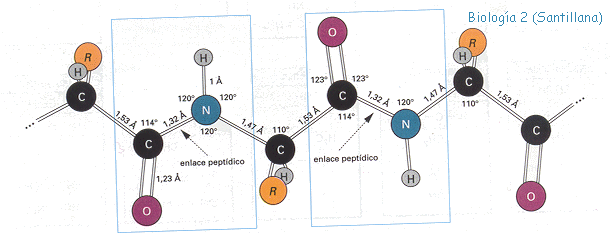
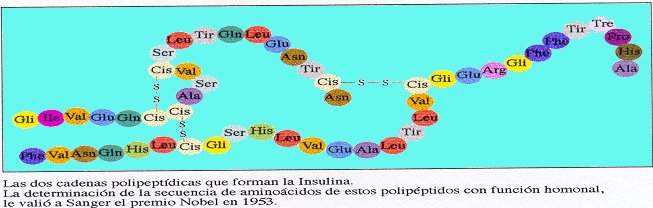
Estructura primaria. La estructura primaria de las proteínas
se refiere a la secuencia de aminoácidos., es decir, la combinación lineal de
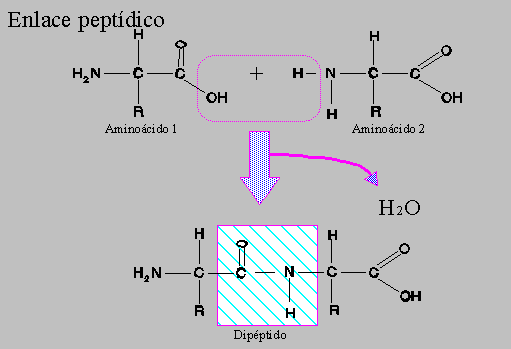
los aminoácidos mediante un tipo de enlace covalente, el enlace peptídico. Los
aminoácidos están unidos por enlaces peptídicos siendo una de sus
características mas importante la coplanaridad de los radicales constituyentes
del enlace.
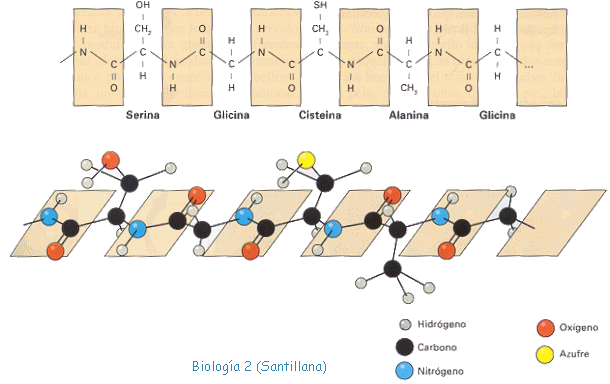
Estructura secundaria. La estructura secundaria de las
proteínas es la disposición espacial local del esqueleto proteico, gracias a la
formación de puentes de hidrógeno entre los átomos que forman el enlace
peptídico, es decir, un tipo de enlace no covalente, sin hacer referencia a la cadena
lateral. Existen diferentes tipos de estructura secundaria: -
Los motivos más comunes son la hélice alfa y la beta lámina
(Hoja plegada beta).
Hélice alfa
Los aminoácidos en una hélice α están dispuestos en una
estructura helicoidal dextrógira, con unos 3.6 aminoácidos por vuelta. Cada
aminoácido supone un giro de unos 100° en la hélice, y los carbonos α de dos
aminoácidos contiguos están separados por 1.5Å. La hélice está estrechamente
empaquetada, de forma que no hay casi espacio libre dentro de la hélice. Todas
las cadenas laterales de los aminoácidos están dispuestas hacia el exterior de
la hélice.6
El grupo amino del aminoácido (n) puede establecer un enlace
de hidrógeno con el grupo carbonilo del aminoácido (n+4). De esta forma, cada
aminoácido (n) de la hélice forma dos puentes de hidrógeno con su enlace
peptídico y el enlace peptídico del aminoácido en (n+4) y en (n-4). En total
son 7 enlaces de hidrógeno por vuelta. Esto estabiliza enormemente la hélice.
Esta dentro de los niveles de organización de la proteína.
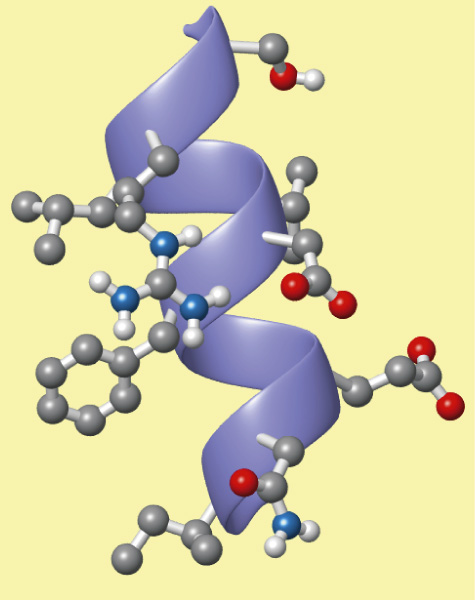
Lámina beta
La beta lámina se forma por el posicionamiento paralelo de
dos cadenas de aminoácidos dentro de la misma proteína, en el que los grupos
amino de una de las cadenas forman enlaces de hidrógeno con los grupos
carboxilo de la opuesta. Es una estructura muy estable que puede llegar a
resultar de una ruptura de los enlaces de hidrógeno durante la formación de la
hélice alfa. Las cadenas laterales de esta estructura están posicionados sobre
y bajo el plano de las láminas. Dichos sustituyentes no deben ser muy grandes,
ni crear un impedimento estérico, ya que se vería afectada la estructura de la
lámina
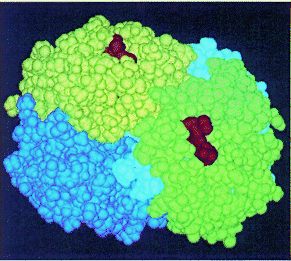
Nivel de dominio.
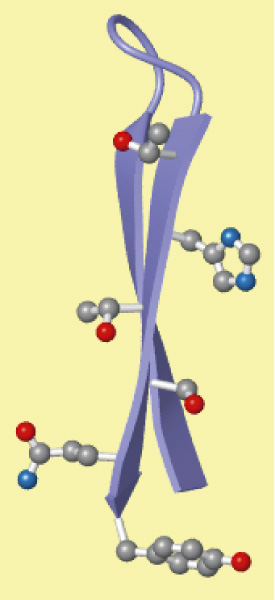
Estructura terciaria. Se llama estructura terciaria a la disposición tridimensional de todos los átomos que componen la proteína.
Se distinguen dos tipos de estructura terciaria:
|












No hay comentarios:
Publicar un comentario